
山东省济南市莱芜区2020年暑假新高三高考一轮化学物质及其变化复习测试含答案
11页1、绝密启用前山东省济南市莱芜区2020年暑假新高三高考一轮化学物质及其变化复习测试本试卷分第卷和第卷两部分,共100分,考试时间90分钟。分卷I一、单选题(共15小题,每小题4.0分,共60分) 1.下列表示对应化学反应的离子方程式正确的是()A 碳酸钙溶于稀醋酸:CaCO3+2H+Ca2+H2O+CO2B 铜与稀硝酸反应:3Cu+2NO3-+8H+3Cu2+2NO+4H2OC 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+H2O+BaCO3D 用银氨溶液检验乙醛中的醛基:CH3CHO+Ag(NH3)2+2OH-CH3COO-+NH4+NH3+Ag+H2O2.一种白色固体可能由Na+、Ba2+,Cl-,Br-、HC、S、S离子中的若干种组成,陶宝同学设计实验检验其组成,记录如下:下列关于固体组成的结论错误的是()A 肯定含有Br-,可能含有HCB 至少含有S、S中的一种离子C 肯定不含Ba2+,一定含有Cl-D 无需焰色反应即可断定溶液中含有Na+3.下列各组离子或分子在溶液中能大量共存,且满足相应要求的是()4.下列有关离子检验的操作和实验结论都正确的是
2、()5.一定质量的某铁的氧化物FexOy,与足量4 molL-1稀硝酸溶液充分反应,消耗硝酸700 mL,放出2.24 L NO气体(标准状况)。则该铁的氧化物的化学式为()A FeOB Fe2O3C Fe3O4D Fe8O106.甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如下图(反应条件及其它产物已略去)。下列说法不正确的是( )A 若甲是AlCl3溶液,则丁可能是NaOH溶液B 若甲是Fe,则丁可能是Cl2C 若丁是CO2,则甲可能为MgD 若丁是O2,则乙、丙的相对分子质量可能相差167.常温下,下列各组离子在指定溶液中一定能大量共存的是( )A 滴入酚酞呈无色的溶液中:K、Al3、Cl、CO32-B 澄清的溶液中:Na、K、MnO4、AlO2C10-13molL1的溶液:Na、Ag(NH3)2、OH、NO3Dc(I)0.1 molL1的溶液中:Na、H、ClO、SO42-8.下列各组离子在溶液中能大量共存,但不能使溴水褪色的是()A Na、Ba2、Cl、OHB Na、K、S2、SOC H、Na、SO、NOD K、Ca2、SO、SO9.下列说法不正确的是()A 为了
3、提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO47H2O进行消毒、净化,以改善水质B 铝表面有一层致密的氧化薄膜,故铝制容器可用来腌制咸菜等C 从分类的角度看,混合物、分散系、胶体的从属关系如图所示:D 借助扫描隧道显微镜,应用STM技术可实现对原子或分子的操纵10.下列说法不正确的是()A234U,235U,238U是不同的核素,互称同位素B 陶瓷,玻璃,水晶,红宝石都属于硅酸盐C Na与熔融的KCl反应能制取K,但不能证明Na的金属性比K强D 在400,800个大气压下,钠能与二氧化碳生成钻石和石墨,反应过程中CO2被还原11.根据下表提供的数据可知,在溶液中能大量共存的微粒组是()A H2CO3,HCO3,CH3COO,CNB HCO3,CH3COOH,CN,CO32C HCN,HCO3,CN,CO32D HCN,HCO3,CH3COO,CN12.分类是化学学习中经常用到的方法,下列对一些物质或化学反应的分类以及依据正确的是()A H2SO4是酸,因为H2SO4中含有氢元素B 豆浆是胶体,因为豆浆中的分散质粒子直径在1100 nm之间C Na和H2O的反应不是离子反应
4、,因为反应中没有离子参加D Na在Cl2中燃烧不是氧化还原反应,因为没有得氧或失氧13.下列各组离子在溶液中能大量共存,加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是()A Ba2+、N、N、Cl-B Ca2+、HC、N、AlC K+、Ba2+、Cl-、HSD Mg2+、N、S、K+14.在溶液中能大量共存的一组离子或分子是( )A NH4、H、NO3、HCO3B K+、Al3+、SO42、NH3H2OC Na+、K+、SO32、Cl2D Na+、CH3COO、CO3+、OH-15.在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是()A a反应:Fe2+2H+H2O2=Fe3+2H2OB b反应:HC+OH-=C+H2OC c反应:H+OH-=H2OD d反应:Al3+3NH3H2O=Al(OH)3+3N分卷II二、非选择题(共4小题,每小题10.0分,共40分) 16.含氮废水进入水体中对环境造成的污染越来越严重。某校环保小组的同学认为可以用金属铝将水中的N还原成N2,从而消除氮污染。(1)配平以下有关的离子反应方程式:N+Al+H2ON2+Al(
《山东省济南市莱芜区2020年暑假新高三高考一轮化学物质及其变化复习测试含答案》由会员jinz****ang分享,可在线阅读,更多相关《山东省济南市莱芜区2020年暑假新高三高考一轮化学物质及其变化复习测试含答案》请在金锄头文库上搜索。

鲁教版(五四制)七年级上册 1.2 图形的全等 学案(无答案)

鲁教版(五四制)七年级上册 1.3 探索三角形全等的条件(第三课时)学案(无答案)
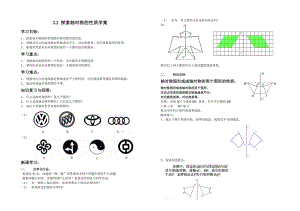
鲁教版(五四制)七年级上册2.2探索轴对称的性质学案(无答案)

鲁教版(五四制)七年级上册第一章 三角形章末复习学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第一课时)学案 (无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第四课时)学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第三课时)学案(无答案)

鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第二课时)学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第二课时)学案

鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第一课时)学案(无答案)

鲁教版(五四制)七年级上册 1.1 认识三角形(第五课时)学案(无答案)

鲁教版(五四制)七年级上册1.4三角形的尺规作图学案(无答案)

鲁教版(五四制)七年级上册1.5利用三角形全等测距离学案(无答案)

鲁教版(五四制)七年级上册2.1轴对称现象学案(无答案)
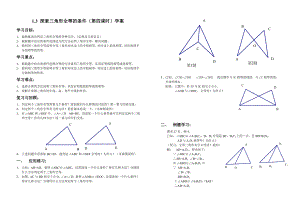
鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第四课时)学案(无答案)

教师版-江苏省盱眙县实验中学苏科版九年级数学上册导学案(训练案)2.2-1圆的对称性

人教版初中化学讲义——16 第六单元 一氧化碳、二氧化碳、制取二氧化碳

教师版-江苏省盱眙县实验中学苏科版九年级数学上册导学案(训练案)2.7弧长及扇形的面积

人教版初中化学讲义——11化合价规律、相对分子质量、质量分数计算

高考 保分班话术
 2013高中物理7-9实验验证机械能守恒定律同步检测新人教版必修
2013高中物理7-9实验验证机械能守恒定律同步检测新人教版必修
2023-04-27 7页
 《小数的初步认识》测试及答案
《小数的初步认识》测试及答案
2022-10-27 5页
 四川省三台中学实验学校高一数学5月月考试题
四川省三台中学实验学校高一数学5月月考试题
2022-08-20 10页
 上海高中生物会考知识点整理(全)
上海高中生物会考知识点整理(全)
2023-09-20 21页
 湖北省武汉市两校2017-2018学年高一化学10月联考试题
湖北省武汉市两校2017-2018学年高一化学10月联考试题
2023-06-14 6页
 2015-2016高中生物第一单元第二章第一节细胞的化学组成学案无答案中图版必修1
2015-2016高中生物第一单元第二章第一节细胞的化学组成学案无答案中图版必修1
2023-03-12 4页
 2013高考生物 考点预测分析 细胞的分化、衰老和凋亡(含解析)新人教版
2013高考生物 考点预测分析 细胞的分化、衰老和凋亡(含解析)新人教版
2023-12-31 7页
 高二化学选修4知识点总结
高二化学选修4知识点总结
2023-07-06 11页
 江西省吉安市凤凰中学2014高二数学 小题训练 理(5月13日实验班) 新人教A版
江西省吉安市凤凰中学2014高二数学 小题训练 理(5月13日实验班) 新人教A版
2023-02-09 2页
 高二语文参考答案
高二语文参考答案
2023-10-22 4页

