
高考总复习课程--高考化学第二轮复习(江苏版)讲义册子 第18讲 化学实验探究2019新题赏析
4页1、第18讲 化学实验探究2017新题赏析题一:重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 FeOCr2O3,还含有硅、铝等杂质。制备流程如图所示:回答下列问题:(1)步骤的主要反应为:FeOCr2O3 +Na2CO3+NaNO3Na2CrO4+Fe2O3+CO2+NaNO2上述反应配平后FeOCr2O3与 NaNO3的系数比为_。该步骤不能使用陶瓷容器,原因是_。(2)滤渣1中含量最多的金属元素是_,滤渣2的主要成分是_及含硅杂质。(3)步骤调滤液2的 pH 使之变_(填“大”或“小”),原因是_(用离子方程式表示)。(4)有关物质的溶解度如图所示。向“滤液 3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到_(填标号)得到的K2Cr2O7固体产品最多。a. 80 b. 60 c. 40 d. 10步骤的反应类型是_。(5)某工厂用 m1 kg铬铁矿粉(含Cr2O3 40%)制备 K2Cr2O7,最终得到产品 m2 kg,产率为_。题二:以工业生产硼砂所得废渣硼镁泥为原料制取MgSO47H2O 的过程如图所示:硼镁泥的主要成分如下表:回答
2、下列问题:(1)“酸解”时应该加入的酸是_,“滤渣1”中主要含有_(写化学式)。(2)“除杂”时加入次氯酸钙、氧化镁的作用分别是_、 _ 。(3)判断“除杂”基本完成的检验方法是_。(4)分离滤渣3应趁热过滤的原因是_。题三:1溴丙烷是一种重要的有机合成中间体,沸点为71,密度为1.36 gcm-3。实验室制备少量1溴丙烷的主要步骤如下: 步骤 1: 在仪器 A 中加入搅拌磁子、12 g 正丙醇及 20 mL水,冰水冷却下缓慢加入 28 mL浓H2SO4;冷却至室温,搅拌下加入 24 g NaBr。步骤 2: 如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。 步骤 3: 将馏出液转入分液漏斗,分出有机相。步骤 4: 将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL 5% Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得1溴丙烷。(1)仪器 A 的名称是_;加入搅拌磁子的目的是搅拌和_。 (2)反应时生成的主要有机副产物有2溴丙烷和_。 (3)步骤2中需向接收瓶内加入少量冰水并置于冰水浴中的目的是_。 (4)步骤2中需缓慢加热使反应和蒸馏平稳进
《高考总复习课程--高考化学第二轮复习(江苏版)讲义册子 第18讲 化学实验探究2019新题赏析》由会员tang****xu2分享,可在线阅读,更多相关《高考总复习课程--高考化学第二轮复习(江苏版)讲义册子 第18讲 化学实验探究2019新题赏析》请在金锄头文库上搜索。

探矿权申请登记书及申请书格式1非油气探矿权新立申请登记书

水运工程重点建设项目质量鉴定申请书

机械行业隐患检查表

水泥、砂石、掺加剂、配合比、土工检测委托合同单

求职新人面试的必胜9要点管理资料

氧气安全使用操作规程模板

水电建筑及设备安装工程价格指数说明

水利水电工程监理工作考核实施细则

水资源管理方案信息平台软件需求说明书4目录
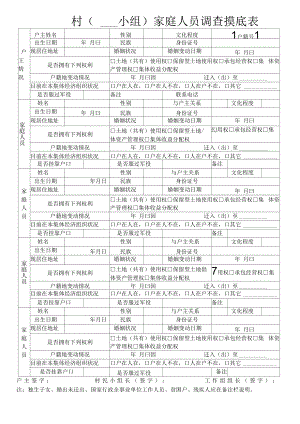
村小组家庭人员调查摸底表
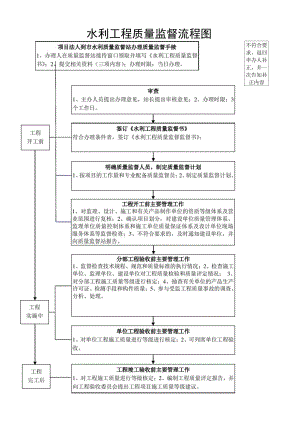
水利工程质量监督流程图

水产养殖用药减量行动情况统计表

水体旅游景观有些含义与类别工程
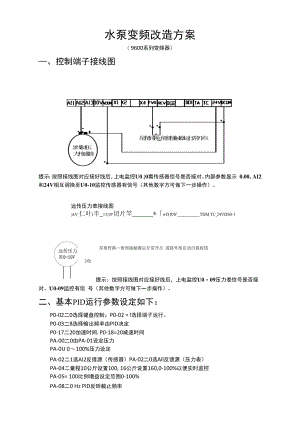
水泵变频改造方案

水泥车间一期循环风机叶轮的投标说明各潜在的投标商

求职介绍信五篇(最新)

永不言败的励志名言大全

氧气说课原稿

村委会常用证明格式模板

求职面试最易犯的错误管理资料
 小数数学题:简便计算11道练习题及参考答案A10
小数数学题:简便计算11道练习题及参考答案A10
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A7
小数数学题:简便计算11道练习题及参考答案A7
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A3
小数数学题:简便计算11道练习题及参考答案A3
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A5
小数数学题:简便计算11道练习题及参考答案A5
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A9
小数数学题:简便计算11道练习题及参考答案A9
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A6
小数数学题:简便计算11道练习题及参考答案A6
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A8
小数数学题:简便计算11道练习题及参考答案A8
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A1
小数数学题:简便计算11道练习题及参考答案A1
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A4
小数数学题:简便计算11道练习题及参考答案A4
2024-04-17 2页
 小数数学题:简便计算11道练习题及参考答案A2
小数数学题:简便计算11道练习题及参考答案A2
2024-04-17 2页

