
04级冶金物理化学期末辅导
54页1、冶金物理化学学习指导及习题解答1冶金热力学辅导热力学内容下四个部分1) 冶金热力学基础2) 冶金熔体(铁溶液、渣溶液)3) 热力学状态图(Ellingham 图,相图)注:把各个知识点划分成三个等级;最重要的等级“重点掌握”第二等级“掌握” ,第三等级“了解” ,这便于学习者在自学或复习内容时参考。也便于在学习时能抓住重点,更快更好地掌握冶金物理化学这门重要基础学科。1 1 冶金热力学基础共 7 个知识点1) 重点掌握体系中组元 i 的自由能表述方法;(包括理想气体、液体、固体)理想气体的吉布斯自由能封闭的多元理想气体组成的气相体系中,任一组元 i 的吉布斯自由能为lniiiGRTPiiP 组分气体的实际压强, ; 标准压强, ,也即 。i aPaPa51032.应该注意的是,高温冶金过程中的气体由于压强比较低,都可以近似看作理想气体。液相体系中组元 i 的吉布斯自由能在多元液相体系中,任一组元 i 的吉布斯自由能为lniiiGRTa其中, -组元的活度,其标准态的一般确定原则是:ia若 i 在铁液中,选 1%溶液为标准态,其中的浓度为质量百分数,%i;若 i 在熔渣中,选纯物质为标准
2、态,其中的浓度为摩尔分数, ;iX若 i 是铁溶液中的组元铁,在其他组元浓度很小时,组元铁的活度定义为 1。固相体系中组元 i 的吉布斯自由能在多元固相体系中,其中任一组元 i 的吉布斯自由能为lniiiGRTa确定原则是:ia若体系是固溶体,则 i 在固溶体中的活度选纯物质为标准态,其浓度为摩尔分数,;iX若体系是共晶体,则 i 在共晶体中的活度定义为 1;若体系是纯固体 i,则其活度定义为 1。2)重点掌握化学反应等温方程式lnGRTQ有三种情况 1) ,以上反应不可以自动进行;0G2) ,以上反应可以自动进行;3) ,以上反应达到平衡,此时RTLnK注:(1) 是反应产物与反应物的自由能的差,表示反应的方向(反应能否发生的判据) ;GcdCDabABQ表示任意时刻(不平衡状态 )的压强商或活度商。(2) 是反应产物与反应物处于标准态时自由能的差,表示反应的限度(反应平衡态的度量) 。 的关系式,建立了体系处于标准态时能量差和处于平衡态时GRTLnK各组元量的关系。是反应的平衡常数。 KcdDabAB其中,组元 A、B、C、D 有三种情况(1)若组元是固态时, (i=A,B,C,D
3、) ;1i(2) 若组元是气态时, ,而 是组元 i 的无量纲分压;iiPai(3)若组元存在与液态中, 表示组元 i 的活度。其中,在一般情况下i若 i 在金属溶液中,活度的标准态选 1%;若 i 在炉渣中,则选纯物质为标准态。3)重点掌握 Vant Hoff 等压方程式2lndKHTR这即是 Vant Hoff 等压方程式的微分式。若上式的 为常数,可以得出积分式如H下:或lnKBTlA其中,B 是不定积分常数,A 也是常数。上式两边同乘-RT,亦可改变为lnRTHBR其中,左边为 ,右边 为常数,用 a 表示,BR 常数用 b 表示,则得GHabT4)掌握用定积分法和不定积分计算 及fGr定积分结果: 2982980122TSTaMbcM 其中 1ln0MT21 232 9862298TM, , , 均可由手册查出。01不定积分法结果2306TPbcHCdaTT 0lnGI式中 及 为积分常数,由以下方法确定:I1).用 T=298K 时的已知的 值,通过上式可以求出 ;298H0H2).用 T=298K 时的已知的 值与已知的 求出 ,用 1)中求出的 代入,298S298G0
4、H可求出 。I5)掌握由物质的标准生成吉布斯自由能 及标准溶解吉布斯自由f能 ,求化学反应的solGrG定义 f恒温下,由标准大气压( )下的最稳定单质生成标准大气压( )1mol 某物质时反PP应的自由能差。 注:稳定单质的 0f定义 solG 恒温下,某一元素 M 溶解在溶剂中,形成 1(质量)的溶液时自由能的变化。一般为 。)%(1质 量solGabT用 及 计算 的通式: (或 ) fGsolrrifiGsoli-化学反应方程式中反应物 i 或产物 i 的计量系数,若 i 代表反应物,则 为“” ;i i若 i 代表产物,则 为“+” (注:以下类同) 。i6)掌握由吉布斯自由能函数求 rG焓函数 定义 为焓函数TRH自由能函数 定义 为自由能函数,记为TRGfe参考温度下无知的标准焓RH如果为气态物质,则 为 0K 标准焓,记为 ;RH0H如果为凝聚态物质,则 为 298K 标准焓,记为 。298自由能函数 计算ferG反应过程的 iff()TRrHrTrRG得 rTrRHfe注:当参加反应的物质既有气态又有凝聚态,将 统一到 298K。298K 与 0K 之间的自RH由能函
《04级冶金物理化学期末辅导》由会员壹****1分享,可在线阅读,更多相关《04级冶金物理化学期末辅导》请在金锄头文库上搜索。

校长培训工作总结(4篇).doc

承德旅游职业学院教(学)案

大学生村官个人述职汇报_1

电解与库仑习题解答

苏教版六年级数学小升初检测卷含答案解析

图书管理系统

“问题探究式”教学模式及案例

个人自我评价简短

校园植树节活动总结

初中道德与法治单音与和声教学设计学情分析教材分析课后反思

人教版小学六年级英语下册期末试题及答案

2022寒假社会实践感受

写家乡风景700字作文

植树节活动总结摘选

大学英语预备级2课后练习翻译答案

证券从业《证券市场基本法律法规》考核题库含参考答案38

小升初浓度问题专题

高考数学大二轮总复习增分策略专题四数列推理与证明第1讲等差数列与等比数列试题

桂科版小学信息技术四年级上册全册教案
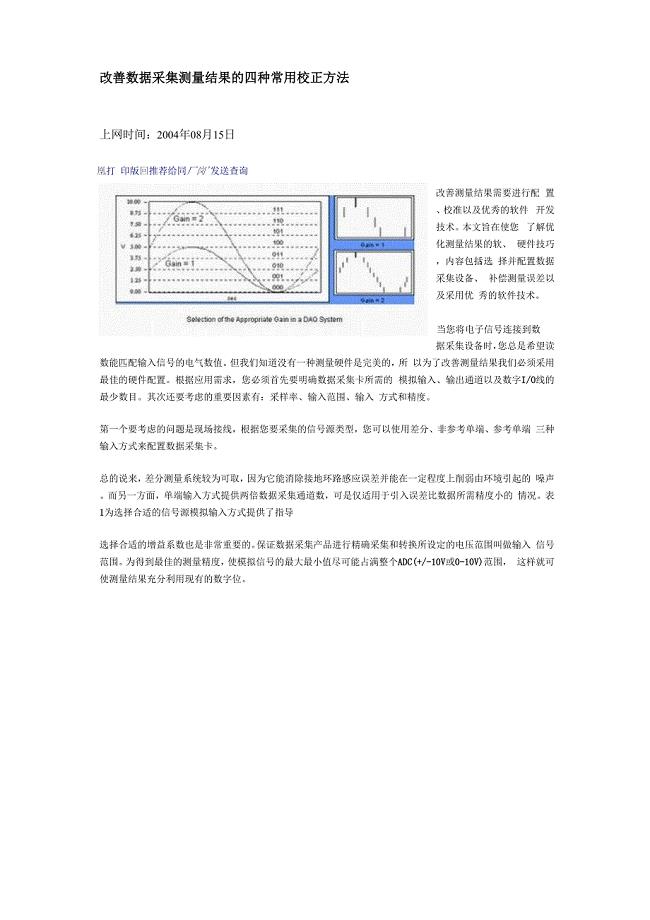
改善数据采集测量结果的四种常用校正方法
 支吊架设计指导
支吊架设计指导
2024-03-01 2页
 水管补偿器选型计算书
水管补偿器选型计算书
2024-03-01 7页
 危化品现场隐患排查速查手册
危化品现场隐患排查速查手册
2024-02-02 47页
 塔式起重机安装、使用、拆卸监理实施细则
塔式起重机安装、使用、拆卸监理实施细则
2024-02-02 9页
 社区护理课程:社区灾害的急救及急、重症病人的转诊服务练习测试题附答案
社区护理课程:社区灾害的急救及急、重症病人的转诊服务练习测试题附答案
2024-02-02 5页
 项目部春节期间安全保证措施
项目部春节期间安全保证措施
2024-02-02 5页
 设计变更与工程签证与确认单与工程洽商与联系单与会签的区别
设计变更与工程签证与确认单与工程洽商与联系单与会签的区别
2024-02-02 9页
 企业安全管理基本工作解读
企业安全管理基本工作解读
2024-02-01 142页
 2023化工有限责任公司生产安全事故应急预案专家评审通过
2023化工有限责任公司生产安全事故应急预案专家评审通过
2024-02-01 162页
 地下顶管施工方案
地下顶管施工方案
2023-09-13 52页

